Ecuación de Estado
La ecuación que describe normalmente la relación entre la presión, el volumen, la temperatura y la cantidad (en moles) de un gas ideal es:
Donde:
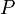 = Presión absoluta
= Presión absoluta = Volumen
= Volumen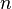 = Moles de gas
= Moles de gas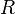 = Constante universal de los gases ideales
= Constante universal de los gases ideales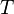 = Temperatura absoluta
= Temperatura absoluta
Ecuacion de Van Der Waals
Haciendo una corrección a la ecuación de estado de un gas ideal, es decir, tomando en cuenta las fuerzas intermoleculares y volúmenes intermoleculares finitos, se obtiene la ecuación para gases reales, también llamada ecuación de Van der Waals:
Donde:
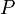 = Presión del gas
= Presión del gas = Volumen del gas
= Volumen del gas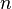 = Número de moles de gas
= Número de moles de gas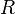 = Constante universal de los gases ideales
= Constante universal de los gases ideales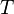 = Temperatura del gas
= Temperatura del gas y
y 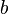 son constantes determinadas por la naturaleza del gas con el fin de que haya la mayor congruencia posible entre la ecuación de los gases reales y el comportamiento observado experimentalmente.
son constantes determinadas por la naturaleza del gas con el fin de que haya la mayor congruencia posible entre la ecuación de los gases reales y el comportamiento observado experimentalmente.
Ecuacion General de los Gases Ideales:
Partiendo de la ecuación de estado:
Tenemos que:
Donde R es la constante universal de los gases ideales, luego para dos estados del mismo gas, 1 y 2:
Para una misma masa gaseosa (por tanto, el número de moles «n» es constante), podemos afirmar que existe una constante directamente proporcional a la presión y volumen del gas, e inversamente proporcional a su temperatura.
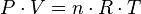

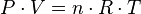
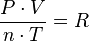


No hay comentarios.:
Publicar un comentario